Puntuación:

- Cada respuesta correcta suma 1/2 punto.
- Cada respuesta incorrecta (o múltiple) resta 1/6 punto.
- Cada pregunta no contestada no puntúa.
Resulta conveniente contestar solamente aquellas preguntas cuya
respuesta se conozca con seguridad. Sólo hay una respuesta correcta en
cada pregunta.
En la hoja de respuestas no olvidéis rellenar:
- NOMBRE Y APELLIDOS.
- DNI.
- MODELO (Importante: toda hoja de respuestas sin modelo
equivale a un suspenso).
- Un átomo excitado puede volver a su estado fundamental por dos caminos distintos.
En el primero, pasa a un estado intermedio emitiendo radiación de longitud de
onda
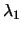 y después al fundamental emitiendo radiación de longitud de
onda
y después al fundamental emitiendo radiación de longitud de
onda 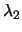 . En el segundo camino, pasa directamente al estado fundamental
emitiendo radiación de longitud de onda
. En el segundo camino, pasa directamente al estado fundamental
emitiendo radiación de longitud de onda 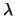 .
¿Cuál será la relación entre
.
¿Cuál será la relación entre 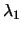 ,
, 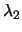 y
y 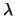 ?
?
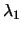 +
+ 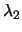 =
= 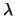
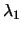 -
- 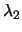 =
= 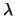
-
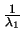 +
+
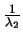 =
=
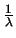
-
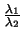 =
=
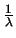
- La energía de ionización (o función de trabajo) del potasio metálico
es menor que la del niquel metálico. Indica cuál de las siguientes afirmaciones
será correcta:
- La longitud de onda crítica (o umbral) para el K es mayor que para el Ni.
- La frecuencia crítica (o umbral) del Ni es menor que para el K.
- La energía de ionización de estos metales no puede relacionarse
con sus propiedades fotoeléctricas.
- Un electrón liberado del K por luz de una cierta frecuencia tiene una
velocidad menor que un electrón liberado del Ni por luz de la misma frecuencia.
- Las propiedades ondulatorias de una partícula se hacen más patentes:
- al aumentar su velocidad.
- al aumentar su momento lineal.
- al disminuir su energía cinética.
- al disminuir su longitud de onda de de Broglie.
- Un átomo en un estado excitado tiene un tiempo de vida de 10 ns. La
energía del estado excitado:
- se puede medir con tanta precisión como se quiera.
- se puede medir con un error mayor que 10
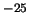 J.
J.
- no se puede medir.
- se puede medir con un error menor que 10
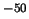 J.
J.
- Para una partícula de masa
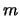 que se mueve en la dimensión X,
el operador
que se mueve en la dimensión X,
el operador 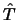 es
es
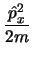 .
Para este caso, el conmutador
.
Para este caso, el conmutador
![$
\left[\hat{T},\hat{p}_x\right]
$](img15.gif) vale
vale
- 1
- -1
- 0
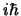
- Una función de onda válida para una partícula libre de masa
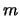 moviéndose en el eje
moviéndose en el eje 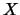 es
es
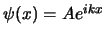 .
Esta función:
.
Esta función:
- Es autofunción del operador momento lineal (
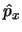 )
con autovalor
)
con autovalor 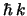 .
.
- Es autofunción del operador momento lineal (
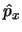 )
con autovalor
)
con autovalor 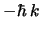 .
.
- Es autofunción del operador momento lineal (
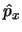 )
con autovalor 0.
)
con autovalor 0.
- No es autofunción del operador momento lineal (
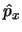 ).
).
Nota:
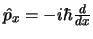 .
.
- Dada la función de onda
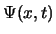 que cumple que
que cumple que
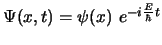 ,
podemos decir de ella que:
,
podemos decir de ella que:
- no es solución de la ecuación de Schrödinger dependiente del
tiempo.
- la densidad de probabilidad que describe no depende del tiempo.
- describe estados no estacionarios del sistema.
- describe un sistema en el cual la energía
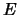 depende del tiempo.
depende del tiempo.
- Las funciones
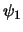 y
y 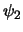 son autofunciones del operador
son autofunciones del operador
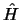 con autovalores
con autovalores 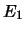 y
y  , respectivamente.
Una función de onda
, respectivamente.
Una función de onda
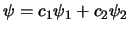 con
con 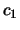 y
y 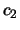 distintos de 0,
distintos de 0,
- siempre es autofunción de
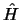 .
.
- nunca es autofunción de
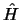 .
.
- es autofunción de
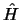 sólo si
sólo si 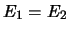 .
.
- a veces es autofunción de
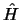 , con autovalor
, con autovalor
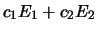 .
.
- ¿Cuál de las siguientes partículas es más probable que
atraviese una barrera de potencial de 1 eV de altura por efecto túnel?
- Un electrón con una energía de 0.1 eV.
- Un electrón con una energía de 0.9 eV.
- Un protón con una energía de 0.1 eV.
- Un protón con una energía de 0.9 eV.
- Cuando una partícula confinada en una caja monodimensional de longitud
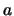 se encuentra en un estado descrito por la función de onda
se encuentra en un estado descrito por la función de onda
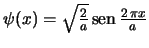 (
(
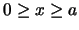 )
)
- La densidad de probabilidad de encontrarla en
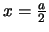 es nula.
es nula.
- La densidad de probabilidad de encontrarla en
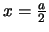 es
mayor que en
es
mayor que en
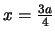 .
.
- La densidad de probabilidad de encontrarla en
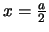 es
mayor que en
es
mayor que en
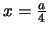 .
.
- La probablidad de encontrarla en
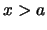 no es nula.
no es nula.
- Si podemos escribir
la energía del sistema se puede expresar como
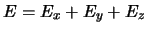
- si
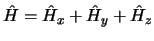 .
.
- si
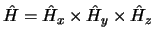 .
.
- siempre.
- si
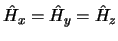 .
.
- De un electrón que se encuentra en el orbital
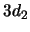 del átomo de hidrógeno
sabemos que
del átomo de hidrógeno
sabemos que
- El módulo de su momento angular orbital vale
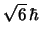 y su componente
y su componente 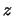 vale
vale
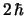 .
.
- El módulo de su momento angular orbital vale
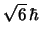 y su componente
y su componente 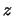 vale
vale
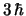 .
.
- El módulo de su momento angular orbital vale
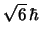 y sus componentes
y sus componentes 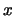 ,
, 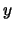 y
y 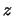 valen
valen
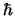 ,
, 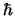 y
y 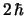 , respectivamente
, respectivamente
- El módulo de su momento angular orbital vale
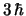 y su componente
y su componente 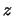 vale
vale
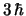 .
.
- Los números cuánticos correspondientes al orbital de un átomo hidrogenoide
siguiente
son:
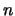 = 2,
= 2, 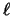 = 1,
= 1, 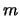 = 1
= 1
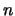 = 2,
= 2, 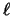 = 1,
= 1, 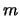 = 0
= 0
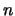 = 3,
= 3, 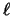 = 2,
= 2, 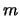 = -1
= -1
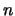 = 2,
= 2, 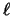 = 3,
= 3, 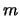 = 1
= 1
- ¿Cuál de las siguientes transiciones entre orbitales de un átomo hidrogenoide
corresponde a una transición permitida de la serie de Balmer?
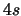
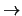
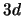
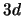
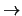
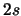
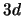
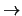
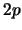
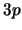
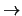
- Considerese la función de onda del estado fundamental del átomo de helio.
- La función de onda completa no cambia de signo al intercambiar las
coordenadas de dos electrones.
- La función de onda completa debe ser antisimétrica al intercambiar las
coordenadas de dos electrones.
- La función de onda completa debe ser simétrica al intercambiar las
coordenadas de dos electrones.
- La función de onda completa sólo depende de las coordenadas
espaciales.
- ¿Cuál de las siguientes funciones puede usarse para representar correctamente
un estado del átomo de Li?
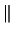
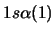
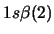
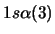
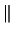
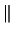
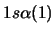
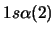
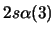
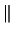
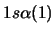
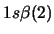
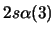
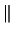
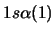
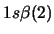
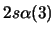
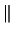
Nota: La nomenclatura
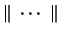 representa un determinante de Slater formado a partir
de los spin-orbitales reseñados.
representa un determinante de Slater formado a partir
de los spin-orbitales reseñados.
- El término espectral fundamental para el átomo de Zr
([Kr], 4
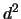 5
5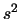 ) es:
) es:
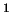 P
P
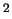 D
D
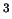 F
F
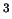 D
D
- El hamiltoniano electrónico de la molécula de LiH
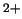 , donde los subíndices 1 y
2 denotan los electrones, es:
, donde los subíndices 1 y
2 denotan los electrones, es:
-
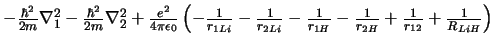
-
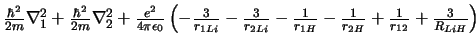
-
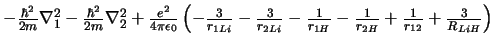
-
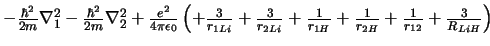
- La aproximación de Born-Oppenheimer implica que:
- la energía de los núcleos es cero.
- se puede tratar el movimiento de los electrones sin tener en cuenta la
posición de los núcleos.
- la velocidad de movimiento de los electrones es menor que la de los núcleos.
- la energía potencial bajo la que se mueven los núcleos surge de
resolver la ecuación de Schrödinger electrónica.
Hay que elegir una de las siguientes preguntas
- Si la curva de energía electrónica frente a R (distancia internuclear) en una
molécula diatómica no posee un mínimo,
- el estado descrito es enlazante.
- el estado descrito es antienlazante.
- podemos calcular la distancia de enlace.
- la energía de disociación de la molécula es muy pequeña.
- La configuración electrónica del estado fundamental de la molécula diatómica
B
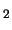 es (
es (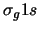 )
)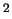 (
(
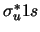 )
)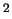 (
(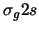 )
)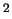 (
(
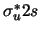 )
)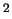 (
(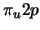 )
)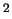 . Teniendo en cuenta únicamente el
orden de enlace, ¿cuál de las siguientes afirmaciones es correcta?
. Teniendo en cuenta únicamente el
orden de enlace, ¿cuál de las siguientes afirmaciones es correcta?
- El ion positivo B
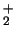 tiene una energía de disociación mayor
que la de la molécula neutra B
tiene una energía de disociación mayor
que la de la molécula neutra B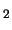 .
.
- El ion positivo B
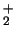 tiene una energía de disociación menor
que la de la molécula neutra B
tiene una energía de disociación menor
que la de la molécula neutra B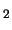 .
.
- El ion negativo B
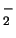 tiene una energía de disociación menor
que la de la molécula neutra B
tiene una energía de disociación menor
que la de la molécula neutra B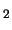 .
.
- Esta molécula es necesariamente inestable.
© Copyright.
Alfredo Aguado
2005-07-11

